

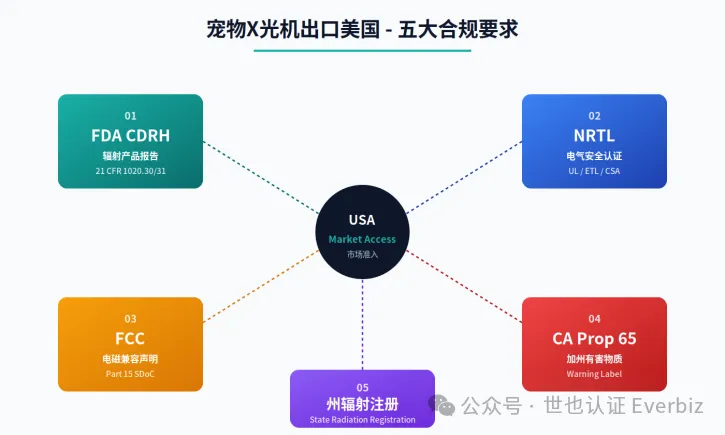
一、五大合规要求一图看懂
宠物用X光机(Veterinary X-ray)虽然不属于FDA对人用医疗器械的510(k)管辖范围,但作为电离辐射发射设备,仍然要满足美国多个联邦机构和州政府的合规要求。
二、FDA CDRH 辐射产品报告(最容易被忽视的强制项)
▎ 为什么兽用X光机也要管FDA?
很多厂家以为 "FDA只管人用医疗器械",这个理解只对了一半。FDA下设的 CDRH(Center for Devices and Radiological Health,器械与放射健康中心)有两条独立的管理线:
医疗器械线:针对人用医疗器械,通过510(k)、PMA等路径管理。兽用产品确实不走这条线。
电子产品辐射控制线:依据 21 CFR Subchapter J(Parts 1000-1050),管理所有发射电离辐射或非电离辐射的电子产品。无论人用兽用,只要是X射线设备,都受这条线管辖。

▎ FDA 辐射产品报告提交流程
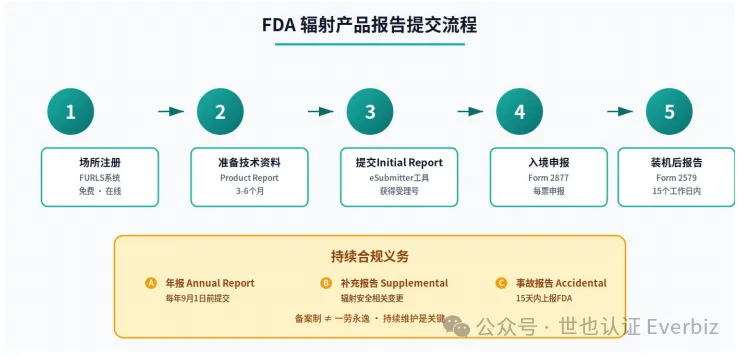
第一步:场所注册
(Establishment Registration)
登录: FDA FURLS 系统
(https://www.access.fda.gov/oaa/)
选择类别: Radiation-Emitting Electronic Product Registration(注意:不是医疗器械注册)
费用: 目前免费
需要注册: 制造商 + 美国 Initial Importer(初始进口商)
第二步:准备 Product Report 技术资料
依据 21 CFR 1002.10,Product Report 需包含内容:
产品识别信息(品牌、型号、用途说明)
技术规格(球管参数、高压发生器、限束器、探测器等)
逐条对应 21 CFR 1020.30 与 1020.31 的合规说明
辐射安全测试报告(曝光重现性、线性度、kV准确度等)
质量控制程序与关键部件溯源文件
认证标签、警告标签、铭牌样张
英文用户手册(包含21 CFR 1020.30(h)(3)要求的辐射安全章节)
第三步:提交 Initial Report
推荐工具:FDA 官方免费工具 CDRH eSubmitter,选择模板 "Diagnostic X-ray System"
提交方式:通过CDRH Portal 在线上传或邮寄到 FDA Document Control Center
FDA 处理:辐射产品报告是备案制(不是审批制),提交后会获得 Accession Number(受理号),后续所有报告都要引用此号

第四步:海关入境申报(Form 2877)
每一票货物入境美国时,进口商或报关行需提交 FDA Form 2877(Declaration for Imported Electronic Products),申明产品符合辐射安全标准并填写 Accession Number。
第五步:装机后报告(Form 2579)
依据 21 CFR 1020.30(d),每一台 X 射线系统在终端用户处完成安装后的 15 个工作日内,装配者(经销商或本地工程师)必须向 FDA 和州辐射控制部门各提交一份 FDA Form 2579,内容包括主部件序列号、安装日期、安装地址等。
▎ 时间与成本预估
准备完整 Initial Report:3-6 个月(取决于测试报告准备进度)
提交到获得Accession Number:1-2 个月
委托代理服务费:市场行情约USD 5,000-15,000(一次性,不含测试费)+ 年报维护费
三、NRTL 电气安全认证
NRTL(Nationally Recognized Testing Laboratory)是美国职业安全与健康管理局(OSHA)认可的测试机构。OSHA 要求美国工作场所使用的电气设备必须经 NRTL 认证。
▎ 适用标准
UL 61010-1:实验室、测量与控制设备的电气安全通用标准— 兽用 X 光机最常采用的路线
UL 61010-2-091:含X 射线柜的实验室设备专用补充标准
ANSI/AAMI ES60601-1 + IEC 60601-2-54:如果按医疗设备路线走(兽用通常不强制),可参考人用设备的 60601 系列

四、FCC 电磁兼容声明
FCC(联邦通信委员会)对所有进入美国市场的电子设备都有 EMC(电磁兼容)要求。即使产品不带任何无线功能(如 WiFi/蓝牙),作为数字电子设备仍属于 "非有意辐射体"(Unintentional Radiator),受 FCC Part 15 Subpart B 管辖。
▎ 不同设备的 FCC 路径

五、加州 Proposition 65
加州第65号提案(简称 Prop 65 或 CA65)要求在加州销售的任何产品,如果含有州政府清单中的特定有害物质(目前清单超过 900 种,包括铅、镉、邻苯二甲酸酯、镍化合物等),且暴露量超过安全阈值时,必须在产品上加贴黄色警告标签。
▎ X 光机相关的高风险物质
铅(Lead):X 光机的铅屏蔽件、限束器、铅玻璃等都含铅,是 Prop 65 重点管控物质
镉(Cadmium):部分电池、焊料、涂层中可能含镉
邻苯二甲酸酯类(Phthalates):常用于电缆、塑料外壳、密封件中
镍化合物:金属电镀层、不锈钢部件等警告标签。

六、州辐射设备注册(易被忽略的最后一公里)
除联邦层面的 FDA 辐射产品报告外,美国大部分州还要求 X 射线设备在使用所在州的辐射控制部门单独注册。这个责任主要在终端用户(医院、诊所),但作为制造商需要提供必要的支持文件。
▎ 典型州辐射注册要求
加州:Radiologic Health Branch (RHB) 注册
纽约州:Department of Health Bureau of Environmental Radiation Protection 注册
德州:Texas Department of State Health Services 注册
佛罗里达州:Bureau of Radiation Control 注册制造商需要为每一台出货的设备提供
FDA Form 2579(Assembler's Report)模板与填写指引
Accession Number 与认证标签信息
主部件(球管、发生器、限束器、探测器)的序列号清单
辐射输出参数表
七、八个最容易踩的坑
1. 以为兽用就不归 FDA 管
21 CFR Subchapter J 管所有 X 射线设备,无论人用兽用。
2. 拿了 NRTL认证就以为万事大吉
NRTL 管电气安全,FDA 管辐射安全,是两条独立合规线,缺一不可。
3. 没有美国 Initial Importer
FDA 要求每个出口的辐射产品必须有美国境内的初始进口商作为责任方。
4. 忘记每年提交 Annual Report
每年 9 月 1 日前要提交,内容包括上一年度销售量、投诉、变更汇总等。
5. 设计变更不报告 FDA
球管、限束器、控制软件等辐射相关变更必须提交 Supplemental Report,否则原 Accession Number 失效。
6. 标签缺少 "For Veterinary Use Only" 标识
兽用标识不清晰会被海关或 FDA 误判为人用,触发 510(k) 要求。
7. 忽略 Prop 65 警告标签
即使不在加州销售,产品可能被加州终端用户转售;加州律师事务所有专门的 "赏金猎人" 团队。
8. 装机后不提交 Form 2579
21 CFR 1020.30(d) 明确要求 15 个工作日内提交,逾期是合规缺陷,在 FDA 检查时会被记录。

EVERBIZ — 您的医疗器械全球市场准入伙伴
EVERBIZ 专注医疗器械全球市场准入合规服务,深耕兽用与人用 X 射线设备多年,已成功协助多家国内厂家实现产品出海美国、欧盟、加拿大、日本等主要市场。
▎ 我们的核心服务
1. FDA 注册申报全流程
辐射产品报告(Initial Product Report)编制与提交
510(k)、De Novo、PMA 等医疗器械路径申报
FURLS 系统场所注册与年度维护
年报、补充报告、事故报告持续维护
Form 2877、Form 2579 模板与填写辅导
2. NRTL 安全认证
UL、ETL、CSA、TÜV 等 NRTL 实验室对接
UL 61010 系列、IEC/UL 60601 系列测试辅导
差距分析(Gap Analysis)与整改方案
技术文件编制与审核
3. EMC / FCC 测试与申报
FCC Part 15 Subpart B SDoC 编制
EMC 预测试与正式测试对接
整改对策与设计建议
4. 加州 Prop 65 合规
化学物质风险评估
警告标签设计(Short-form / Long-form)
供应链物质溯源支持
5. 美国代理人(U.S. Agent)与 Initial Importer 服务
美国境内法定代理人服务
Initial Importer 注册与代办
FDA 检查应对支持
6. 标签与英文 IFU 编制
符合 21 CFR 1020.30 要求的认证、警告、铭牌设计
英文用户手册编制(包含强制性辐射安全章节)
Quick Reference Card、安装手册等配套文件
7. 50 州辐射设备注册支持
各州辐射控制部门注册要求差异化分析
Assembler's Report 模板与培训
装机现场支持(部分地区)
8. 其他全球市场准入服务
欧盟 MDR / IVDR 合规
加拿大Health Canada MDL
日本PMDA、韩国 MFDS、巴西 ANVISA 注册
中国 NMPA 注册




